Lotus 2015
Trinkwasserdesinfektion – weltweit von zentraler
Bedeutung
Um Wasser zu desinfizieren und somit für den menschlichen Gebrauch mikrobiologisch sicher zu machen, werden weltweit unterschiedliche Methoden angewandt., die sich in zwei Gruppen aufteilen lassen.
Physikalische Methoden
Zu den physikalischen Methoden zählt zunächst erst einmal die Filtration. Deren einfachste und am weitesten verbreitete Form ist die Filtration von Grundwasser durch die verschiedenen geologischen Schichten im Boden, sowie in den Filteranlagen von Wasserwerken mit ihren zahlreichen Kies- und Sandschichten.
Weitere Arten der Filtration sind die sogenannte Ultrafiltration bishin zur Sterilfiltration. Beide Verfahren bleiben aber eher speziellen Bereichen der Wasseraufbereitung vorbehalten. Zu den physikalischen Methoden zählt auch die Bestrahlung des Wassers mittels UV-Licht. Die sogenannte UV-Entkeimung hat die Vorteile, dass es ein relativ kostengünstiges Verfahren ist und auch schwer zu bekämpfende Parasiten wie Giardia oder Cryptosporidien mit dieser Methode zuverlässig deaktiviert werden.
Jedoch ist allen physikalischen Desinfektionsmethoden gemeinsam, dass sie nur als Barriere eingesetzt werden können und über keinerlei Depotwirkung verfügen. Sie sind somit nur eine erste Behandlungsstufe in einem umfassenden Aufbereitungsverfahren.
Chemische Methoden
Bei chemischen Desinfektionsmethoden wird das Wasser mit einem hochreaktiven Oxidationsmittel versetzt. In der Trinkwasseraufbereitung sind hierzu nur Chemikalien erlaubt, deren Konzentration überwachbar und deren Gefährdungspotenzial für die menschliche Gesundheit bekannt und kalkulierbar sind.
Ein Nebeneffekt aller dieser Desinfektionsmittel ist, dass sie nicht nur spezifisch auf die zu bekämpfenden Mikroorganismen wirken, sondern auch mit anderen Inhaltsstoffen des Wassers reagieren. So können im Zuge ihrer Chemie auch u.U. unerwünschte Reaktionsprodukte entstehen. Das Ziel einer chemischen Desinfektion muss also die Optimierung des Verfahrens sein, um das mikrobiologische Risiko so gut wie möglich zu minimieren, ohne das durch die Desinfektionsnebenprodukte ein neues Risiko entsteht.
Chlor – weltweit verwendet, aber mit vielen Nachteilen
Das weltweit gebräuchlichste chemische Desinfektionsmittel für Wasser ist – weil preiswert und leicht verfügbar – Chlor. Es hat in der Bevölkerung eine hohe Akzeptanz. Gleichgültig welche Ausgangschemikalie verwendet wird: Der aktiv desinfizierende Teil davon ist die hypochlorige Säure. Chlorgas dissoziiert in Wasser zu hypochloriger Säure und Salzsäure.
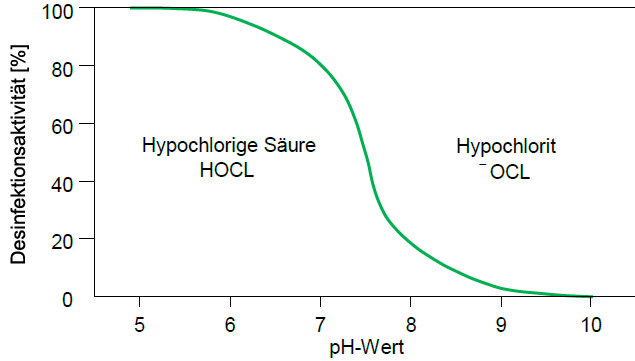
In der stark alkalischen Chlorbleichlauge (Natriumhypochloritlösung) liegt das Chlor in Form des für die Desinfektion fast unwirksamen Hypochlorit-Anions vor. Erst bei Absenkung des pH-Wertes unter pH 9 entsteht hypochlorige Säure, mit der die Chemikalie seine desinfizierende Wirkung entfalten kann. Aus diesem Gleichgewicht zwischen Chlorgas, Hypochloriger Säure und Hypochlorit erklärt sich die starke Abhängigkeit der Desinfektionswirkung vom pH-Wert.
Trinkwasser darf einen pH-Wert zwischen 6,5 und 9,5 haben. Bei erhöhten pH-Werten gerät man aber schnell in einen Bereich mit mangelhafter Desinfektionssicherheit, obwohl vermeintlich ausreichende Chlorkonzentrationen nachweisbar sind.
Zudem können Aufgrund seiner hohen, aber unspezifischen Reaktivität bei der Wasserdesinfektion mit Chlor zahlreiche unerwünschte Desinfektionsnebenprodukte entstehen. Ammonium wird beispielsweise – je nach Reaktionsbedingungen – zu Mono-, Di- oder Trichloramin chloriert. Aber auch eine Vielzahl von organischen Substanzen neigt dazu, chloriert zu werden. Wasser erhält dadurch gesundheitsgefährdende oder geschmacksverschlechternde Eigenschaften. Hierzu gehören beispielsweise die als krebserregend verdächtigten Trihalogenmethane (THM), die besonders in Huminstoff enthaltenden Wässern auftreten, oder die in der Getränkeindustrie gefürchteten Chlorphenole.
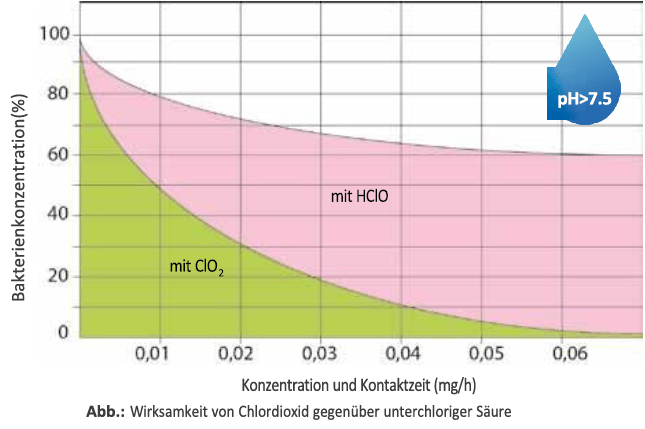
Chloridioxid – Desinfektion mit höchster Effizienz
Chlordioxid weist gegenüber dem in der Wasserdesinfektion hauptsächlich eingesetzten Chlor aufgrund seiner Chemie eine Reihe von Vorteilen auf.
Chlordioxid dissoziiert nicht wie Chlor, sondern löst sich als grünlich-gelbes Gas in Wasser. Dadurch ist seine Desinfektionswirkung unabhängig vom pH-Wert.
Die gebräuchlichste Methode zur Herstellung von Chlordioxid ist das so genannte „Chlorit-Säure-Verfahren“. Chlordioxidlösung wird aus Natriumchlorit (NaClO2) und Salzsäure (HCl) nach folgender Gleichung erzeugt:
5 NaClO2 + 4 HCl =
4 ClO2 + 5 NaCl + 2 H2O
Natriumchlorit + Salzsäure =
Chlordioxid + Kochsalz (NaCl) + Wasser
Aufgrund seines sehr hohen Redox-Potentials ist
Chlordioxid erheblich effektiver als andere Desinfektionsmittel, wie z.B. Chlor. Deshalb ist eine deutlich geringere Konzentration für die gleiche Desinfektionswirkung ausreichend.
Ein weiterer Vorteil ist seine Langzeitstabilität in Leitungssystemen von mehreren Tagen gegenüber Chlor von nur einigen Stunden. Darüber hinaus baut Chlordioxid im Gegensatz zu Chlor aktiv Biofilme in Leitungen und Behältern ab. Dadurch ist ein besserer Schutz von Wassersystemen und vor allen Dingen die Bekämpfung von Legionellen möglich. Weder reagiert es mit Ammonium noch bilden sich chlorierte Nebenprodukte wie z.B. die als krebserregend verdächtigten Trihalogenmethane (THM).
Warum Chlordioxid?
Chlordioxid ist ein hoch wirksames Desinfektionsmittel
– gegen Legionellen und andere pathogene, Chlor resistente Keime
– mit einem hohen Eindringungsvermögen in Biofilme über einen weiten pH-Bereich
– und sorgt durch seine Langzeitstabilität für viele Stunden bis Tage für einen mikrobiologischen Schutz im Leitungsnetz – ohne Zehrung durch im Wasser gelöstes Ammonium
– ohne Bildung von Chlorphenolen und anderer, geruchsintensiver Verbindungen
– ohne Bildung von Trihalogenmethanen (THM) und anderen chlorierten Kohlenwasserstoffen (AOX).